本站讯 近日,中国海洋大学医药学院、海洋药物教育部重点实验室江涛教授联合香港大学李学臣教授,在国际知名学术期刊Science Advances在线发表题为“Achieving cysteine-selective peptide/protein bioconjugation via tunable triazine-pyridine chemistry”(通过可调控的三嗪-吡啶化学实现肽/蛋白中半胱氨酸的选择性偶联)的研究文章。
蛋白/肽的化学标记是理解蛋白/多肽功能、研发抗体/肽偶联药物、设计靶向药物的关键技术和基础科学问题,是化学与医学和生命科学连接的桥梁。特异性地在多肽或蛋白的特定位点引入化学修饰或功能基团的技术,不仅为揭示生命过程的分子机制提供了有力工具,也为基础研究向应用的转化搭建了桥梁。从阐明蛋白质结构与功能的动态关联,到开发高效靶向的抗体偶联药物,蛋白/多肽的选择性偶联凭借其精确性、灵活性和高效性,持续拓展着多肽与蛋白质的应用边界,展现出推动未来新兴生物技术产业发展的巨大潜力。
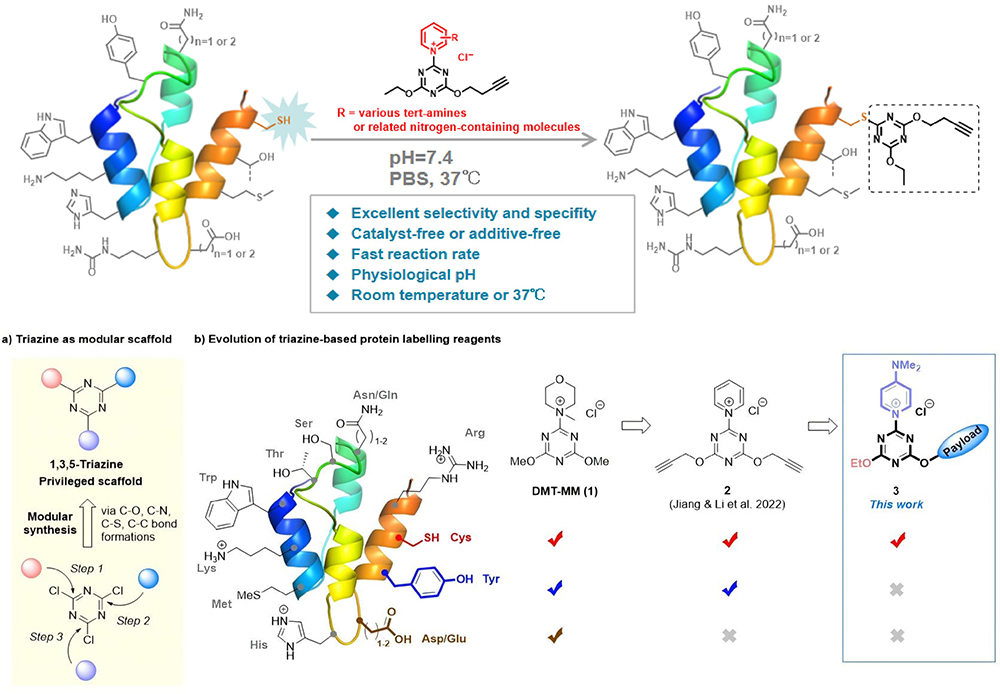
图1 多肽/蛋白中半胱氨酸的化学修饰策略
研究团队在2022年首次报道了能够选择性偶联酪氨酸的三嗪-吡啶鎓化学(TPC)探针,成功实现了在全蛋白质组水平上对酪氨酸的特异性标记(Chem. Commun., 2022, 58, 7066)。在本研究工作中,团队开发了一种在生理条件下能够对多肽/蛋白中半胱氨酸(Cys)实现选择性偶联的探针。机理研究表明,探针引入对位N,N-二甲基氨基吡啶基是实现这一高选择性的关键,且C-N键解离能与Cys选择性呈正相关,这为理性设计提供了理论依据。优化所得的最佳试剂9b成功应用于曲妥珠单抗的Cys选择性标记,可在还原条件下特异性修饰链间二硫键并保持抗体活性。该方法支持构建多位点、高载药量的ADC,其产物在人血浆中的稳定性显著优于传统方法,为开发新一代稳定、可控的生物偶联药物提供了新策略。
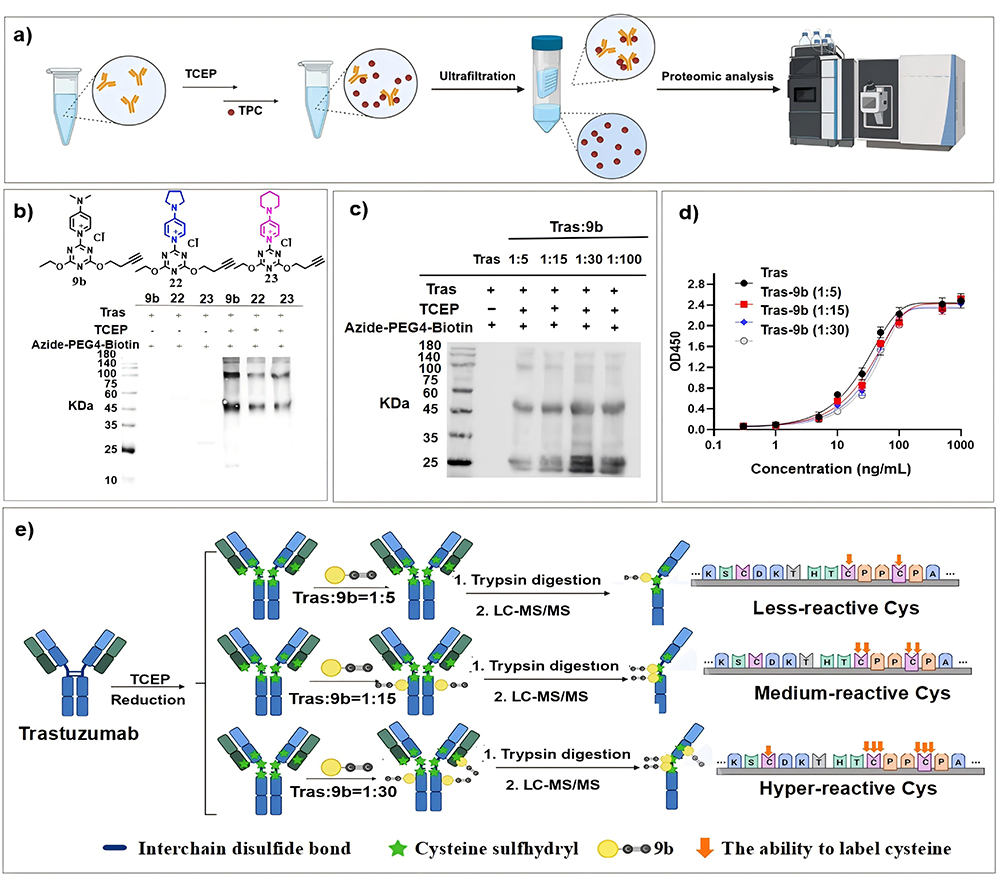
图2 曲妥珠单抗中链间半胱氨酸的选择性偶联
研究团队还将三嗪-吡啶化学的选择性偶联,成功应用于肽偶联药物(PDC)研究。相关成果以“Conjugating 10,11-Dimethoxy-camptothecin with an Integrin αvβ3-Targeting Peptide through a Triazine Linker for Targeted Tumor Treatment in Lung and Pancreatic Carcinoma”(通过三嗪连接子将10,11-二甲氧基喜树碱与整合素αvβ3靶向肽偶联用于肺癌和胰腺癌的靶向治疗)为题,发表在学术期刊Journal of Medicinal Chemistry。肽偶联药物的挑战是其在体内循环系统中不稳定,导致偶联的药物(Payload)释放引起体内毒性。研究团队通过三嗪环连接子的引入,设计合成PDC-2肽偶联物在血浆中展现出高稳定性,并可通过整合素αvβ3介导的内化途径,表现出强的肿瘤细胞靶向性和对肿瘤细胞的强抑制活性。机制研究表明,PDC-2能够同时下调Survivin蛋白的表达并抑制PI3K/AKT/mTOR信号通路。在整合素αvβ3过表达的肺癌A549和胰腺癌AsPC-1 的小鼠模型中, PDC-2显示出更优的肿瘤生长抑制效果和肿瘤靶向特异性,以及更低的系统性毒性。药代动力学分析表明,PDC-2可实现母体药物的持续释放,将其半衰期延长了3.4倍,并促进药物在肿瘤组织中的特异性蓄积。综上所述,PDC-2在肺癌和胰腺癌治疗中展现出良好的应用前景,是一种有潜力的候选药物。

图3 多肽偶联药物研究的示意图

江涛教授课题组(第一排右五为江涛教授)
中国海洋大学为上述研究的第一完成单位,医药学院江涛教授、香港大学李学臣教授为Science Advances文章的共同通讯作者,中国海洋大学毕业博士生王朝明与青岛海洋生物医药研究院尹瑞娟研究员为共同第一作者。医药学院江涛教授与李静教授为Journal of Medicinal Chemistry文章的共同通讯作者,王朝明与张静博士为共同第一作者。研究工作得到了国家自然科学基金和粤港澳大湾区精准医学研究院(广州)重点项目等资助。
文章链接:https://www.science.org/doi/10.1126/sciadv.aea6904
https://pubs.acs.org/doi/10.1021/acs.jmedchem.5c02059
编辑:赵奚赟
责任编辑:刘莅




































